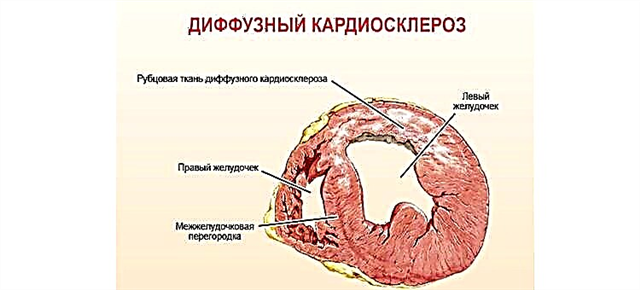
心臓の欠陥は、その構造または大きな血管のいずれかに欠陥があることを特徴とする病気の大きなグループです。
心臓の欠陥とは何ですか
心臓の欠陥が何であるかを理解するには、この臓器の解剖学の基本とその働きの原理を理解する必要があります。
人間の心臓は、4つの心房(2つの心房と2つの心室)で構成されています。血液は、バルブのある穴を通って1つのチャンバーから別のチャンバーに移動します。左心室から、血液は体循環(大動脈)に放出され、私たちの体のすべての器官と組織を酸素化し、大静脈を通って左心房に戻ります。そこから右心室に行き、次に肺動脈に行き、肺の酸素を濃縮し、肺静脈を通って右心房に戻り、次に左心室に戻ります。その後、サイクルが繰り返されます。
心臓内の動脈血と静脈血の混合を防ぐために、左と右のセクションは心房と心室中隔によって分離されています。血液の逆流(心室から心房へ、または大動脈から左心室へ)を防ぐために、特定の時間に開閉するバルブがあります。

すべての心臓の欠陥は、先天性と後天性の2つのタイプに分けられます。
名前が示すように、先天性欠損症は生まれた時から人に現れ、後天性欠損症は後の人生の過程で発生します。
先天性心疾患(CHD)の発生率は、1000人の子供あたり約5〜8例です。後天性心疾患(ACD)は、人口10万人あたり100〜150人に発生します。
CHDとPPSの違いを理解しやすくするために、最初に異常が発生したり、主血管(大動脈と肺動脈幹)の変形や中隔の欠陥が発生したり、後天性の血管が影響を受けたりすることに注意してください。しかし、先天性の欠陥があってもバルブが損傷する可能性があるため、このような分割は任意と見なすことができます。
これはすべて、心臓内の血行動態(正常な血流)の違反、一部のチャンバーでの血液充填の優勢、および他のチャンバーの貧困につながります。その結果、動脈血が静脈血と混ざり合い、特定のチャンバーが血液で溢れ、伸び、壁が厚くなります。逆に、心臓の他の部分の充満は、標準と比較して減少します。
心臓病のほとんどの人は障害者クラスを取得します。すべての健康な人のように、彼らは完全な生活を送ることができません、彼らは常にある種の制限を守る必要があります。純粋に心理的にさえそれは難しいです。
軍隊の問題について-心臓の欠陥を持つ人々は、緊急の兵役に「不適格」または「部分的に適合」に分類されます。
病理学で死ぬことは可能ですか?
残念ながら、心臓病による死亡という事実はかなりあり得ます。先天性心疾患による死亡の統計はかなり悲しいです。タイムリーな医学的介入がなければ、それは症例の70-80%で発生します。
PPPのある人は、症例の約15〜20%で死亡します。心臓病の主な死因は心不全です。 「ポンプ」の主な機能の低下-血液のポンプ。
他の死因には、発作性心室頻脈、心房細動、房室閉塞などの心不整脈が含まれます。心房細動が原因で、血栓塞栓症が脳でしばしば発生し、脳卒中を引き起こします。
考えられる発生原因
後天的な欠陥の原因の中で、最も一般的なものは次のとおりです。
- リウマチ、またはむしろ慢性リウマチ性心臓病は、連鎖球菌感染症(喉の痛み)が(主に小児期に)受けた後に発症する、その内膜(弁装置を含む)の炎症です。
- 感染性心内膜炎は、心臓弁の細菌の増殖による心臓弁の段階的な破壊です。感染のドリフトは、う蝕歯が除去された場合、注射中の皮膚の消毒治療が不十分な場合、または非滅菌注射器を使用した場合に発生する可能性があります。
- アテローム性動脈硬化症と変性弁の変化は、高齢者によく見られます。
よりまれな原因のうち、梅毒と全身性の病状を区別することができます-関節リウマチ、エリテマトーデス、強皮症。
先天性奇形の特定の病因を確立することは困難です。かもね:
- 遺伝性突然変異-ダウン症、パトウ;
- 母体の病気-糖尿病、血栓性素因、全身性血管炎;
- 子宮内ウイルス感染症-風疹、サイトメガロウイルス、水痘;
- 悪習-妊娠中の喫煙、飲酒;
- 電離放射線への曝露;
- 胎児の発育に悪影響を与える薬物の使用-抗腫瘍薬、スルホンアミド、テトラサイクリン。
心臓に欠陥があるかどうかを見分ける方法
人に心臓の欠陥があるかどうかを調べるために、私は次のデータによって導かれます:
- 患者を悩ます症状と苦情;
- 身体的状態-患者の外見;
- 心電図;
- 心エコー検査(心臓の超音波);
- 胸部X線。
患者の症状、徴候および典型的な外観
心疾患のある人は、主に心不全の兆候に苦しんでいます。体が水平になり、肺の血管の圧力が上昇するため、特に夜間は呼吸が困難になります。同じ理由で、発作性咳嗽に悩まされることもあります。
患者(特にCHDの患者)は、身体活動がほとんどない場合でも、すぐに疲れます。常に眠りたいと思っており、めまいを感じ、失神することさえあります。
肝臓が肥大しているため、患者は右季肋部に重さや引っ張り/痛みを感じます。夕方になると、足がとても腫れます。胸の左側の痛み、動悸、胸の不快感を心配することがよくあります。特定のCHDの患者では、下気道感染症が持続します。
先天性心疾患のある人には、いわゆる「ドラムスティック症状」がよく見られます。これは、指の末端指骨の肥厚です。この症状は、全身の血液循環の長期的な違反を示しています。

CHDの新生児と乳児は発育不全で低体重です。多くの場合、唇、鼻、指先は青みがかっています(チアノーゼ)。
心臓病には特定の症状があります。たとえば、大動脈縮窄症では、その顕著な狭窄により、頭、腕、上半身の循環が適切なレベルに保たれ、下半身と脚の血液が枯渇します。これは、上肩帯の筋肉が下肢の未発達の筋肉の背景に対して際立っているという事実につながります。そして、「アスレチックビルド」という誤った印象が生まれます。
別の例は僧帽弁狭窄症です。このPPSの後期では、顔の一般的な蒼白を背景に、明るい青みがかったピンク色の赤面が頬に現れ、唇と鼻は青い色合いになります。これは僧帽弁狭窄症、または僧帽弁顔と呼ばれます。

PPSを患っている人は、長い間非常に健康であり、痛みや呼吸困難を経験することはありません。これは、心臓が血行力学的障害を補償しようとしているという事実によるものであり、最初はこれにうまく対処します。しかし、遅かれ早かれこれらのメカニズムは不十分であり、病気は臨床的に現れ始めます。
そのような患者を診察するとき、私はいくつかの病理学的兆候、例えば、左心室または右心室の心臓インパルスの増加、胸部の震えをなんとか特定することができます。心臓病の患者の聴診中に、私はしばしば弁、中隔、および頸動脈の投射点で雑音を聞きます。トーンを強めたり、弱めたり、分割したりします。
機器診断
心臓の欠陥を診断するための主な機器の研究方法:
- 心電図検査。心電図では、歯の高さ、幅、形状を変えることで、心臓のさまざまな部分に肥大の兆候が見られます。不整脈がしばしば見られます(特にしばしば-心房細動)。
- 心エコー検査は、おそらく心臓の欠陥を確実に確立することを可能にする主要な診断方法です。 Echo-KGは、バルブ、パーティション、壁の厚さ、およびチャンバーの容積の状態を明確に認識します。ドップラーモードでは、部門間の血流の方向(吐き戻し)を確認し、肺動脈の圧力を測定できます。欠陥が疑われる場合は、より詳細な画像として、経食道心エコー図を処方します(トランスデューサーは心臓のすぐ後ろの食道に配置されます)。
- 胸部臓器のX線-写真は、肺動脈幹の膨らみ、肺血管内の圧力の増加による肺パターンの増加、影の形の変化を非常に明確に示しています心臓、肋骨の使用(肋間動脈による圧迫による不均一な輪郭)。
悪徳の種類とその違い
すでに述べたように、すべての心臓の欠陥は先天性と後天性に分けられます。それらは、病態生理学、重症度、平均余命において互いに異なります。
CHDには多くの分類がありますが、ほとんどの場合、臨床医はマーダー分類を使用して、すべてのCHDをチアノーゼのある欠陥とない欠陥(つまり、「青」と「白」)に分割します。
表1.CHDの特性
タイプ | 名前 | 際立った特徴 | 血行力学的障害のメカニズム |
チアノーゼのないCHD (淡いタイプ) | 心室および心房中隔の欠陥 | RVの大幅な増加による「心臓のこぶ」(前胸壁の突出)。胸骨の左側にあるIII-IV肋間腔での激しい収縮期心雑音 | 左から右への血液の排出。 LVの過負荷、次に右心。肺動脈の反射性けいれんによる肺高血圧症の急速な発症 |
動脈管開存症 | 胸骨の左側にあるII-III肋間腔の収縮期拡張期雑音 | 大動脈から肺動脈への血液の排出、小さな円の血流の増加、左心の過負荷 | |
孤立性肺動脈弁狭窄症 | IIトーンの弱化とPAバルブ上の大まかな収縮期心雑音 | 膵臓の急激な過負荷、肺血流の枯渇 | |
大動脈縮窄症 | 高血圧、「運動体格」 「脚の冷え」、下肢の動脈の衰弱または脈動、 胸骨の左端全体に沿ったX線による収縮期心雑音の肋骨の使用 | 大動脈の狭い領域を通る血流の閉塞、左心室の過負荷 | |
チアノーゼを伴うCHD(青色タイプ) | 大血管転位 | 重度の一般的な低酸素症(チアノーゼ、「ばち状核突起」)、心臓のこぶ、頂点で大きなIトーン | 体循環が通過する臓器の酸素不足。 |
心臓の唯一の心室 | 低酸素症の兆候、心尖部の収縮期心雑音 | 動脈血と静脈血の混合、肺血流量の増加、急速な心室過負荷 | |
ファロー四徴症 | 肺動脈上のIIトーンの急激な弱化 | 右から左への血液ダンプ |
後天性心疾患は2つのタイプに分けられます-狭窄、すなわち。チャンバー間の開口部の狭小化、および故障、すなわちバルブの不完全な閉鎖。すべてのPPPは、血液で溢れるいくつかの心腔と他の人の貧困に要約され、その後のすべての結果をもたらします。
成人で最も一般的なAPSは大動脈弁狭窄症です(約80%)。
複合的な欠陥が発生する可能性があります-人が同時に弁の機能不全と狭窄の両方を持っている場合。また、複数のバルブが影響を受けている人を見るのもよくあります。これは、付随する心臓病と呼ばれます。
表2.PPPの特徴
タイプ | 名前 | 際立った特徴 | 血行力学的障害のメカニズム |
僧帽弁(MK)の欠陥 | MKの不足 | Iトーンの弱化、心尖部の収縮期心雑音 | 左心房への血液の逆排出 |
僧帽弁狭窄症 | 大声で私は調子を整え、心尖部で拡張期雑音を出します。僧帽弁。 | 左心房の重度の過負荷、その肥大および拡張。反射性けいれんによる肺血管内の圧力の上昇 | |
大動脈弁(AK)の欠陥 | AKの欠如 | 脈拍血圧の上昇、頸動脈の目に見える脈動、AKでの拡張前の雑音 | 大動脈からの血液の逆流による左心室の膨張 |
大動脈弁狭窄症 | 狭心症に似た痛み、絶え間ない失神。頸動脈に及ぶAKの大まかな収縮期心雑音 | 大動脈への血液排出の悪化、左心室の過負荷 | |
肺動脈(PA)弁の欠陥 | 航空機の不足 | LA弁のIIトーンの弱化、胸骨の左側のII肋間腔での拡張前の雑音 | 右心室への血液の逆排出 |
LA狭窄 | IIトーンの増幅と分割。右心室の顕著な脈動 | LAへの血液の排出の妨害、膵臓の過負荷 | |
三尖弁(TC)の欠陥 | TCの欠如 | TCでの収縮期心雑音 | 右心房への血液の逆排出 |
TC狭窄 | TCでのIトーンの増幅 | 右心房の過負荷、拡張および肥大 |
心臓の欠陥はどのように治療されますか?
残念ながら、心臓病から人を治すことができる薬はありません。そして、すべての先天性心疾患は、手術によってのみ治療されます。例外は動脈管開存症です。これは先天性奇形であり、薬理学的に完全に排除することができます。しかし、これは人の人生の最初の日にのみ有効です。これを行うために、私は非ステロイド性抗炎症薬(イブプロフェン、インドメタシン)の3日間の静脈内注射を処方します。
チアノーゼと重度の心不全の兆候がある場合は、すぐに手術が行われます。多くの場合、外科医は乳児や1歳児でも手術をしなければなりません。器械的研究により欠陥が発見され、患者が何も心配していない場合、または軽微な症状がある場合は、手術を延期することができます。
伝統的に、CHDを排除するための外科的介入は、人工心肺に接続された開心術で全身麻酔下で行われます。欠損は、心膜または合成組織パッチで縫合または閉鎖されます。開いたダクトは結紮または切断されます。
最近、適切な機器を備えた専門の心臓病センターでは、低侵襲の血管内介入を行うことが可能です。このような手術では、超音波とX線の制御下で、右心房に到達する大腿静脈からカテーテルを挿入します。オクルーダーは、ニッケルチタンワイヤーの相互接続されたディスクであるカテーテルを通して挿入されます。このオクルーダーは欠陥を閉じます。
このような手術の主な禁忌は、重度の血管硬化を伴う進行性肺高血圧症です。これらの場合、いわゆる姑息的介入が行われ、それは欠陥自体ではなく、その結果を排除します。大きな血管の間に人工的に作成されたメッセージ(吻合)。これにより、血液が心臓の過負荷部分を循環します。
次に、後天的な欠陥の処理を見てみましょう。それらでは、物事は少し異なります。
リウマチを背景にPPSが発症した場合は、プロトコルに従って、ペニシリン系抗生物質による抗菌療法を確実に使用します。体内に連鎖球菌が存在すると、新しい心臓の欠陥が発生する可能性があるため、この点は非常に重要です。
また、私は常に患者の状態を安定させるのに役立つ薬物療法を処方しています。
まず第一に、心不全の進行を遅らせる薬が使用されます:
- ACE阻害薬-ペリンドプリル、ラミプリル;
- ベータ遮断薬-ビソプロロール、メトプロロール;
- 利尿薬-トラセミド;
- アルドステロン拮抗薬-スピロノラクトン、エプレレノン;
心臓のリズムが乱れる場合は、抗不整脈薬であるソタロール、アミオダロンを使用します。
PPSの一部、特に僧帽弁狭窄症は、左心房に血栓が形成されて心塞栓性脳卒中を引き起こす心房細動を伴うことが多いため、抗凝固療法も重要です。これを防ぐために、私はワルファリンまたは低分子量ヘパリンを処方します。
患者さんが深刻な状態にあるとき、薬が効かなくなったとき、私は患者さんを外科的治療に送ります。
PPPの操作には主に2つのタイプがあります。
- 弁置換術;
- 再建手術-弁形成術、交連切開術、バルーン弁形成術。
人工弁は機械的(人工)および生物学的です。主な違いは次のとおりです。生物学的弁を設置する場合、患者は、手術後の最初の3か月間、および機械的弁の埋め込みを伴う抗凝固療法を一生受ける必要があります。バルブの種類の選択は、毎回個別に決定されます。
人工心臓弁での長期使用が承認されている唯一の抗凝固剤はワルファリンです。
機械式バルブはより耐久性がありますが、そのコストは生物学的バルブよりもはるかに高くなります。
予後を決定するもの:患者はどのくらい生きますか?
私はよく尋ねられます-「彼らは心臓の欠陥を持ってどれくらい生きますか?」
これは、次のような多くの要因に依存します。
- 一種の副;
- その重大度;
- 心不全の程度;
- 合併症の存在;
- 診断と治療の適時性;
- 医師の推奨事項の履行(すべての投与量に準拠した薬物の正しい摂取など);
- 実行された操作の品質。
手術を行わないと、CHDの多い患者は幼児期(2〜5歳まで)に死亡します。人が手術なしで成人期まで生きることができるCHDには、大動脈縮窄症、心房中隔欠損症が含まれます。
予後の観点から最も好ましいPPSは、僧帽弁、三尖弁逆流です。深刻な合併症はめったに発生せず、長い時間が経ちます。他のATS(僧帽弁、大動脈弁狭窄症)では、患者は症状の最初の発症から約5〜10年後に死亡します。
薬理学的手術と心臓手術の両方の最新の治療オプションは、そのような人々の寿命を最大60〜70年延長することができます。
病理学の結果
先天性および後天性の両方の心臓病の患者は、急性心不全(肺水腫、心原性ショック)を発症するリスクが高く、迅速な医学的介入なしでは、人の死につながります。
また、心臓に欠陥のある人は、はるかに早く冠状動脈疾患を発症します。これは、心筋梗塞を発症する可能性が数倍高いことを意味します。
ほとんどすべての心臓の欠陥は、リズム障害を伴います。それらの中で最も危険なのは、心室性頻脈性不整脈と房室閉塞です。
いくつかの欠陥があると、肺循環の顕著な過負荷と肺の反射性血管収縮のために、肺高血圧症が発生します。これは、薬物療法に対応するのが困難な非常に深刻な状態であり、外科的介入が必要です。
全身の顕著な酸素欠乏(低酸素症)が長引くため、免疫系が悪化します。そのため、心臓に欠陥のある患者は、感染症、特に気管支炎や肺炎に絶えず苦しんでいます。
心臓の欠陥や人工弁の存在があると、心臓弁に影響を与える危険な病気である感染性(細菌性)心内膜炎のリスクが数倍になります。
ケーススタディ:大動脈縮窄症のティーンエイジャー
私の実践から興味深い事例を1つ引用します。母親は、幼児期から頭痛、悪寒、および理解できない足の衰弱に悩まされてきた15歳の息子と一緒に私に来ました。 7歳のとき、少年は小児科の病院に入院し、150/90 mmHgまでの高血圧と診断されました。 「高血圧」、処方薬と診断されました。患者は不規則に薬を服用しました。患者の年齢が若く、母親と父親に高血圧がないことから、私は診断を疑うようになり、高血圧の「二次的性質」を疑うようになりました。
患者の一般的な検査中に、血圧の上昇(155/90 mm Hg)に加えて、脚の動脈の脈動の弱まりと、下角のレベルでの背中の収縮期心雑音を特定することができました。肩甲骨の。私は心エコー検査を注文しました。これは、左心室の肥厚と胸部大動脈の狭窄領域を示していました。大動脈縮窄の別の兆候は、レントゲン写真ではっきりと見えました-肋骨の使用(不均一な輪郭)。患者は外科手術を受けました-大動脈の狭くなった領域の形成外科。少年の状態は改善し、血圧は正常に戻り、血圧を矯正するための薬の必要性はなくなりました。
専門家のアドバイス:心臓病と一緒に暮らす
ネガティブな結果のほとんどを回避し、治療の効果を高めるのに役立ついくつかの推奨事項を示したいと思います。
- スポーツ-専門的なトレーニングを停止する必要があります。軽い身体活動は許可されています。
- 定期健診-子供の頃に手術が成功したか、最近軽度の僧帽弁逆流と診断されたかは関係ありません。心臓の欠陥がある場合は、少なくとも6か月または1年に1回心臓専門医を訪問し、ECGおよびEcho-KGを行って心臓機能の状態を確認し、起こりうる合併症の発生を監視する必要があります。
- 食卓塩-慢性心不全の兆候が見られ、その治療のために薬を処方されている場合、その効果を高めるために、食卓塩の使用を1日あたり2〜3グラムに制限する必要があります。
- ワルファリン-この薬は、心臓病の患者の血栓を防ぐために処方されることがよくあります。その受容が効果的であると同時に安全であるために、あなたは定期的に血液検査(凝固図)をする必要があります。この研究のINR指標は、2を超え、3未満である必要があります。
- 耳鼻咽喉科医の診察-リウマチ由来のPPSと診断された場合、リウマチの主な原因は扁桃炎(扁桃炎)であるため、必ず耳鼻咽喉科医に相談してください。慢性扁桃炎の存在下では、扁桃腺の治療(洗浄、抗生物質)が必要であり、おそらくそれらの除去が必要です。これは、リウマチの再発と新しい心臓欠陥の出現を防ぐために必要です。
- 感染性心内膜炎の予防-心臓の欠陥と人工弁を持つすべての人は、感染性心内膜炎を発症するリスクが高くなります。したがって、それを防ぐために、彼らはペニシリン抗生物質(アモキシシリン、アンピシリン)を1回、医療処置(抜歯、気管支鏡検査、膀胱鏡検査など)の約30分/ 1時間前に服用しなければなりません。